PD-1/PD-L1,肿瘤研究小白必知靶点
日期:2019-08-29 11:48:14
近年来,肿瘤免疫治疗(Immunology Oncology Therapy)已成为晚期恶性肿瘤治疗的重要手段之一。肿瘤免疫治疗并不直接攻击癌细胞,而是通过激活人体自身免疫系统来抗击肿瘤,具有良好的安全性及耐受性。PD-1/L1 抗体药物作为肿瘤免疫治疗的代表药物,在晚期恶性肿瘤治疗中取得了巨大的成功。
从2014年,全球首款PD-1抑制剂Opdivo问世开始,到2018年年底,FDA批准了6款PD-1/PD-L1单抗药物,3款PD-1抑制剂。截止至2019年1月8日国家药监局数据库中,PD-1/PD-L1获批了三个产品。为什么PD-1/PD-L1一直备受瞩目,而且热度不减呢?读完本文你将会明白。本文主要从以下几个方面着重介绍:
1. 什么是PD-1/PD-L1?
PD-1的全称是程序性死亡受体-1,属于CD28超家族成员,是由268个氨基酸组成的I型跨膜蛋白。它是在1992年由日本京都大学的Tasuku Honjo教授发现的,可在T细胞、B细胞等免疫细胞表面表达。不过在T细胞未活化时,几乎不表达PD-1,仅在T细胞活化之后,PD-1才在T细胞表面表达。
PD-L1首次被发现是由华裔学者陈列平教授在1999年作为B7家族的第3个成员B7-H1。次年,Tasuku Honjo与哈佛医学院的Gordon Freeman证实B7-H1能够与PD-1结合,抑制T细胞增殖以及细胞因子分泌,负调控淋巴细胞的激活。随后,B7-H1也被更名为程序性死亡受体配体-1(PD-L1)[1]。PD-L1除了会表达在肿瘤表面,参与免疫逃逸,还会在IFN-γ刺激下,表达在抗原提呈细胞(DC细胞、巨噬细胞等),以及血管内皮细胞的表面。
如前所述,PD-1可与PD-L1结合,二者互为受体与配体。但有研究表明,两者并非一对一的关系。PD-1除了能与PD-L1结合,还可以和PD-L2结合。PD-L2也属于B7家族,和PD-L1一样,主要表达在抗原提呈细胞(DC细胞、巨噬细胞等),与PD-1结合后,能够抑制T细胞增殖及细胞因子的产生,与免疫耐受相关。同样的,PD-L1也被发现,可以与其他受体结合,不过目前仍在探索中[2]。
2. PD-1/PD-L1信号通路
T细胞活化依赖于“双信号”系统,第一信号指T细胞受体与主要组织相容性复合物(MHC)的特异性结合,第二信号指抗原递呈细胞(APCs)与T细胞表面的共刺激分子相互作用[3]。负调控共刺激分子通常也被称为免疫检查点,主要用于限制免疫系统的过度激活。
PD-L1作为最重要的免疫检查点之一,除了可组成型低表达于APCs和多种非造血细胞,也可被炎性细胞因子包括干扰素(IFN)、肿瘤坏死因子仅(TNF-α)和血管内皮生长因子(VEGF)等诱导表达。如图所示,在肿瘤微环境中,肿瘤细胞和肿瘤相关APCs高表达PD-L1,肿瘤浸润性淋巴细胞在肿瘤抗原长期刺激下高表达PD-1。PD-L1与PD-1结合后可诱导T细胞凋亡、失能、耗竭,进而抑制肿瘤抗原特异性CD8+T细胞的激活、增殖和抗肿瘤功能,实现肿瘤免疫逃逸[4] [5]。
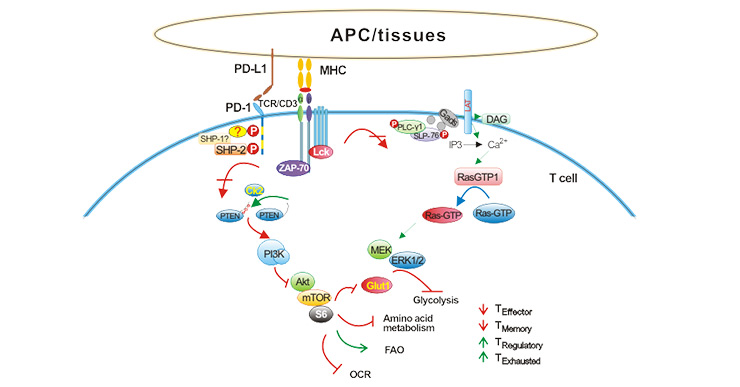
Figure 1. The signaling pathway of PD-1/PD-L1
3. PD-1/PD-L1与肿瘤免疫治疗
肿瘤免疫治疗就是通过重新启动并维持肿瘤-免疫循环,恢复机体正常的抗肿瘤免疫反应,从而控制与清除肿瘤的一种治疗方法。包括单克隆抗体类免疫检查点抑制剂、治疗性抗体、癌症疫苗、细胞治疗和小分子抑制剂等。
近几年,肿瘤免疫治疗的好消息不断,目前已在多种肿瘤如黑色素瘤,非小细胞肺癌、肾癌和前列腺癌等实体瘤的治疗中展示出了强大的抗肿瘤活性,多个肿瘤免疫治疗药物已经获得美国FDA(Food and Drug Administration, FDA)批准临床应用。肿瘤免疫治疗由于其卓越的疗效和创新性,在2013年被《科学》杂志评为年度最重要的科学突破。目前的肿瘤免疫治疗主要是指anti?CTLA?4治疗和anti?PD?1/PD?L1治疗,这里我们具体了解下anti?PD?1/PD?L1治疗。
目前,已在全球上市的6个 PD-1/PD-L1抑制剂均属于大分子抗体类药物。虽然都是利用的抗原抗体结合,但是PD-1和D-L1抗体的作用机制是有区别的。如下图所示,PD-1单抗会与T细胞表面的PD-1结合,阻止PD-1与PD-L1或PD-L2结合,释放被抑制的肿瘤特异的T细胞杀伤能力。而PD-L1抗体,只阻断了PD-L1和PD-1的结合,而对PD-L2和PD-1的结合没有影响 [6] [7]。
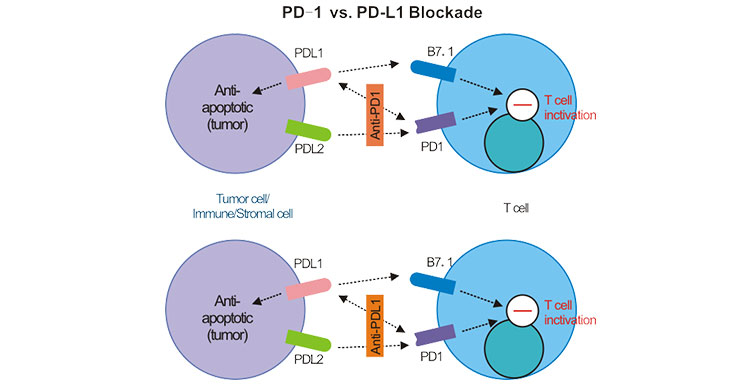
Figure 2. PD-1 vs. PD-L1 Blockade
4. PD-1/PD-L1药物研究进展
目前,已在全球范围内上市并应用的PD-1/PD-L1抗体类药物总共有六个,对应的适应症表一所示,其中Cemiplimab作为全球第3款PD-1抑制剂Cemiplimab(商品名Libtayo)。主要用于治疗转移性皮肤鳞状细胞癌(CSCC)或局部晚期不可切除的CSCC患者。这也是全球唯一一个治疗皮肤鳞状细胞癌的PD-1抑制剂。
Table 1. 已上市PD-1/PD-L1抗体类药物一览表
| 药物名称 | 公司 | 靶点 | 适应症 | 上市日期 |
|---|---|---|---|---|
| Opdivo (Nivolum) | Bristol-Myers | PD-1 | 非小细胞肺癌、恶性黑色素瘤、肾细胞癌、头颈部鳞癌、尿路上皮癌、结直肠癌、肝癌、经典型霍奇金淋巴瘤 | 2014-06 |
| Keytruda (Pembrolizumab) | Merck | PD-1 | 非小细胞肺癌、恶性黑色素瘤、肾细胞癌、头颈部鳞癌、尿路上皮癌、结直肠癌、肝癌、经典型霍奇金淋巴瘤 | 2014-09 |
| Tecentriq (Atezolizu) | Roche | PD-L1 | 非小细胞肺癌、尿路上皮癌 | 2016-10 |
| Bavencio (Avelumab) | Merck and Pfizer | PD-L1 | 梅克尔细胞癌、膀胱癌 | 2017-03 |
| Imfinzi (Durvalumab) | AstraZeneca | PD-L1 | 尿路上皮癌、非小细胞肺癌 | 2017-05 |
| Cemiplimab | Sanofi and Regeneron | PD-1 | 转移性皮肤鳞状细胞癌(CSCC)或局部晚期不可切除的CSCC患者 | 2018-09 |
5. 关于PD-1/PD-L1肿瘤免疫治疗常见问题
结合临床,我们归纳了关于PD-1/PD-L1肿瘤免疫治疗常见的四大问题:
5.1 PD-1/PD-L1单抗是什么药物?
PD-1/PD-L1单抗属于免疫检测点抑制剂,是一种抗体类的肿瘤免疫药物。它的机制是增强体内免疫细胞T细胞对肿瘤细胞的识别,从而达到杀灭肿瘤的作用。可以说,该药物是通过增强我们自身的免疫力去杀伤肿瘤细胞。目前国外批准上市的药物有六种,其中使用最普遍的有三种药物:PD-1单抗opdivo和Keytruda以及PD-L1单抗Tecentriq。这三种药物被广泛用于多种癌种。目前美国FDA批准的癌种覆盖黑色素瘤、肺瘪、肾瘦、霍奇金淋巴瘤、头颈鳞癌和尿路上皮癌。此外,目前也在更多其他癌种开展了临床试验,也取得了不错疗效。
5.2 PD-1/PD-L1单抗如何注射?
Opdivo、Keytruda和Tecentriq均为静脉输注,但具体输注要求略有不同:
(1)Opdivo用0.9%氯化钠注射液或5%葡萄糖稀释,浓度不超过Img/mL-10mg/lmL。小心溶解,勿剧烈摇晃。输液时间超过60min即可。
(2)Keytruda用0.9%氯化钠注射液或5%葡萄糖稀释,浓度不超过Img/mL-10mg/mL。小心溶解,勿剧烈摇晃。输液时间超过30min即可。
(3)Tecentriq用250mL0.9%氯化钠注射液。小心溶解,勿剧烈摇晃。第一次输液时间超过60min,如果耐受,以后每次输液时间超过30min即可。
在注射的过程中监测生命体征,如有不适视具体情况减慢滴速或中断注射。
5.3 PD-1/PD-L1单抗一般多长时间起效?如果有效,需要一直持续应用吗?能否停药?
与问题一中描述的一样,肿瘤免疫类药物是通过增强免疫细胞杀伤肿瘤细胞的间接作用治疾病的,与传统的靶向药相比起效慢些。鉴于免疫治疗起效时间可能在首次用药的3个月之后,因此一些免疫治疗的临床试验要求患者预计生存时间超过12周的条件下才考虑可以入组。NCCN指南里推荐PS评分2分的患者应免疫治疗。
依据目前已有的经验,推荐患者如果治疗有效则长期使用。直到疾病进展,再更换其他治疗方案。有部分患者,在治疗一段时间后达到了CR (疾病完全缓解),并且持续很长一段时间,医生有的时候也会考虑停药。
5.4 PD-1/PD-L1单抗会不会和其他靶向治疗一样产生耐药性?
目前有限的临床数据和随访资料表明,对PD-1/IPD-L1抗体有效的患者,有一部分患者的疾病最终还是会复发,这部分患者可以分为两种:一种是患者用药之后效果很好,停药之后复发,但是再用PD-1抗体还是会有效。这类复发患者并不是真正的耐药。另一种患者是指一类用药还未停止,但是已经消退的肿瘤(达到PR标准)又生长起来的患者。这部分患者目前考虑可能是由于耐药性而复发,患者应及时考虑更换其他治疗方案。
PD-1/PD-L1蛋白
● Recombinant Human Programmed cell death 1 ligand 1(CD274),partial (Active) (Code: CSB-MP878942HU1)

(Tris-Glycine gel) Discontinuous SDS-PAGE (reduced) with 5% enrichment gel and 15% separation gel.
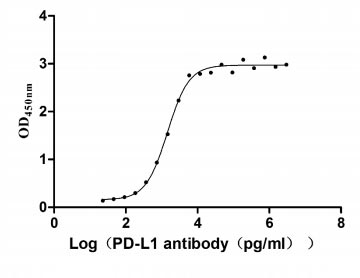
Immobilized PD-L1 at 2 μg/ml can bind Anti- PD-L1 mouse monoclonal antibody(CSB-MA878942A1m, antigen from E.coli), the EC50 of human PD-L1 protein is 1.252-1.653 ng/mL
Reference:
[1] Ribas A. Tumor immunotherapy directed at PD-1 [J]. N Engl J Med. 2012, 366(26):2517-9.
[2] Lieping Chen, et al. Defining and Understanding Adaptive Resistance in Cancer Immunotherapy [J]. Trends Immunol. 2018, 39(8):624-631.
[3] Keir Mary E, ButIe Manish J, et al. PD-l and its ligands in tolerance and immunity [J].Annu Rev Immunol. 2008, 26:677-704.
[4] Boussiotis Vassiliki A. Molecular and biochemical aspects of the PD-l checkpoint pathway [J].N Engl J Med. 2016, 375(18): 1767-1778.
[5] Gordon Sydney R, Maute Roy L, et al.PD-1 expression by tumor-associated macrophages inhibits phagocytosis and tumour immunity [J].Nature. 2017, 545(7655):495-499.
[6] Pardoll DM. The blockade of immune checkpoints in cancer immunotherapy [J]. Nature reviews. Cancer. 2012, 12:252–264.
[7] Weiping Zou, Jedd D. Wolchok, et al. PD-L1 (B7-H1) and PD-1 Pathway Blockade for Cancer Therapy: Mechanisms, Response Biomarkers and Combinations [J]. Sci Transl Med. 2016, 8(328): 328rv4.
上一篇: CD14—细菌脂多糖的膜受体
下一篇: TROP2--肿瘤治疗的重要靶点











