抗体的交叉适应性
日期:2023-07-26 09:25:46
新型冠状病毒SARS-CoV-2自2019年底爆发以来,在全球肆虐,成为研究的热点。经过科学研究人员的不懈努力,已成功开发出几种针对SARS-CoV-2的疫苗。然而,SARS-CoV-2病毒随着时间的推移不断进化,出现了新的变种。人们担心的问题是:这些授权的疫苗是否仍然对新变种有效?专家指出,尽管疫苗的有效性有所降低,但目前的疫苗仍然对新的SARS-CoV-2变种有效。为什么现有的疫苗仍然对SARS-CoV-2的新变种有效?抗体的交叉反应性在一定程度上可以解释这一现象。
1. 交叉反应是什么?
1.1 表位和配位位点
在谈论交叉反应之前,需要提到表位和配位位点。
表位是抗原表面上的特定氨基酸序列(通常只有5-6个氨基酸长),被相应的抗体所识别。表位也被称为抗原决定簇。有些抗原只有一个表位,而其他抗原则有两个或更多不同的表位。
配位位点是抗体变可变区(轻链和重链的顶端部分)的互补结合形成的三维结构。它包含5-10个氨基酸,并且特异性地识别和结合抗原的表位。抗体的Y形结构的每个臂都在N-端具有相同的配位位点。因此,抗体-抗原结合实际上是配位位点和表位之间的相互作用。
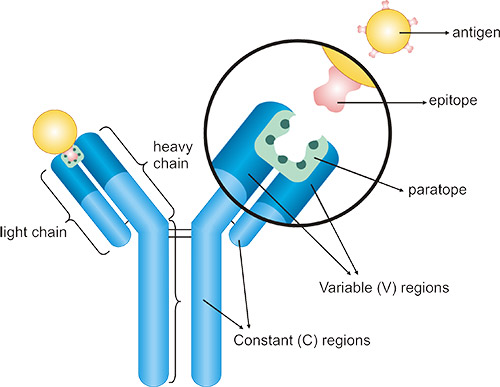
图1. 抗体-抗原结合结构图
1.2 什么是交叉反应?
交叉反应是指抗体与刺激其产生的抗原之外的其他抗原发生反应。这种现象被称为交叉反应。交叉反应是由于多价抗原上的共享表位或表位的构象相似性而发生的。
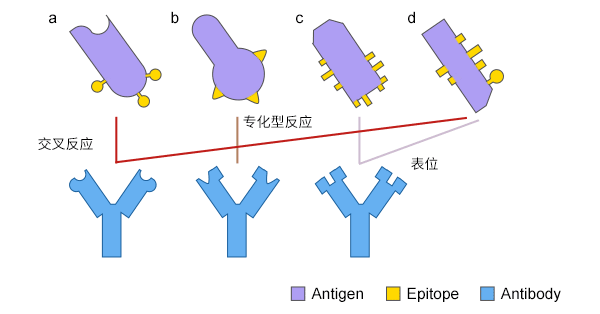
图1. 抗体在两种不同抗原之间的交叉反应
1.3 交叉反应
在免疫学中,交叉反应通常被定义为单个抗体识别不同抗原上相同或结构相似的表位的能力。
2. 交叉反应与特异性的关联与区别
在免疫学中,特异性指的是抗体上的抗位点仅能识别和与相应抗原上的一个特定表位发生作用的能力。需要注意的是,这个独特的表位可能存在于多个抗原上。特异性是由抗原上表位的类型、排列顺序和空间配置确定的。特异性能够精确地检测目标抗原,从而避免测量伪抗原,是免疫应答的最显著特征,也是免疫学中预防和诊断的基础依据。
交叉反应是指抗体识别和结合两个或多个高度同源或具有相同表位的抗原的情况。在免疫分析中,抗体(多克隆抗体)的交叉反应增强了结果的敏感性,并且可以检测到稀有抗原。
特异性评估免疫系统区分不同抗原的能力,而交叉反应评估不同抗原与免疫系统相似程度的程度。在一定程度上,交叉反应大大降低了特异性。
3. 交叉反应的生物学意义
抗体的交叉反应具有防御性和攻击性特征。交叉反应的抗体在自然流行病学中为相关病原菌株或抗原变异提供交叉保护性免疫。换句话说,抗体的防御作用通过交叉反应提供更广泛的免疫保护或对相关病原体提供交叉保护性免疫。有证据显示,抗体的交叉反应是逃避人类多种病原体免疫反应的机制,包括血吸虫病 [1]、流感病毒 [2]和肺炎链球菌 [3]。然而,抗体的交叉反应对宿主可能有害。抗体交叉反应的攻击性作用主要体现在感染性疾病、自身免疫性疾病和过敏的诱导或加重,这是与宿主组织破坏相关的不适当或有害的炎症反应 [4]。在血清学诊断中,抗体的交叉反应会导致特异性诊断或鉴定上的混淆。
此外,交叉反应可能会干扰免疫分析结果并影响重复性。交叉反应可能会在药物滥用筛查测试中导致假阳性干扰,因为抗体对与目标药物具有类似化学结构的另一化合物发生反应 [5] [6]。
4. 交叉反应的应用
交叉反应可以提高抗体的实用性。例如,抗体的交叉反应使其能够检测多个模型生物中同源蛋白质。许多人源抗原衍生的抗体在非人类生物(如小鼠、大鼠和兔子)中显示出显著的交叉反应性,可以用于解释某些免疫病理学现象、诊断某些传染性疾病或诱导对难以制备的抗原的免疫反应。交叉反应可以确认ELISA试剂盒是否特异性检测某个感兴趣的蛋白质。
在临床诊断中,异种抗体检测用于快速检测对致病性单核细胞增多症的病原体—EB病毒产生的抗体 [7]。这些测试利用了抗体的交叉反应性。交叉反应经常被用作评估免疫和蛋白质结合型分析(如ELISA和RIA)的验证参数。
5. 如何避免或减少交叉反应?
测试抗体与密切相关的抗原的交叉反应是一项重要的验证测试。选择适当的抗体是避免免疫分析中交叉反应的最直接解决方案。建议使用mAb作为主抗体(例如用于捕获)以建立高的分析特异性,而应使用pAb作为检测抗体以提高灵敏度。
为了避免交叉过敏反应,患者不得服用与已知引起过敏反应的特定药物具有相似化学结构的药物。红霉素、美司钠、西诺霉素、磺胺甲硝唑和其他大环内酯类药物存在交叉过敏现象。
由于正在开发用于治疗包括癌症在内的广泛疾病的抗体,对交叉反应的充分理解尤为重要。
参考文献:
[1] Fitzsimmons CM, Jones FM, et al. Progressive cross-reactivity in IgE responses: an explanation for the slow development of human immunity to schistosomiasis [J]? Infect. Immun. 2012, 80:4264–4270.
[2] Nara PL, Tobin GJ, et al. How can vaccines against influenza and other viral diseases be made more effective [J]? PLoS Biol. 2010, 8:e1000571.
[3] Väkeväinen M, Eklund C, et al. Cross-reactivity of antibodies to type 6B and 6A polysaccharides of Streptococcus pneumoniae evoked by pneumococcal conjugate vaccines, in infants [J]. J. Infect. Dis. 2001, 184:789–793.
[4] Daria Augustyniak, Grazyna Majkowska-Skrobek, et al. Defensive and Offensive Cross-Reactive Antibodies Elicited by Pathogens: The Good, the Bad and the Ugly [J]. Curr Med Chem. 2017 Nov 24;24(36):4002-4037.
[5] Gagajewski A, Davis GK, et al. False-positive lysergic acid diethylamide immunoassay screen associated with fentanyl medication [J]. Clin Chem. 2002;48:205–6.
[6] Lichtenwalner MR, Mencken T, et al. False-positive immunochemical screen for methadone attributable to metabolites of verapamil [J]. Clin Chem. 1998;44:1039–41.
[7] Tess Marshall-Andon and Peter Heinz. How to use …the Monospot and other heterophile antibody tests [J]. Arch Dis Child Educ Pract Ed. 2017 Aug;102(4):188-193.
上一篇: 标签抗体概述
下一篇: 单抗、多抗、重组抗体应如何选择











