战疫时刻|Th17细胞分化
日期:2020-03-09 11:25:25


Doi:https://doi.org/10.1016/S2213-2600(20)30076-X
研究团队对患者的外周血进行了流式细胞分析。结果显示,血液中CD4和CD8 T细胞的数量大大减少,但它们却被过度激活。
此外,CD4 T细胞中高度促炎性CCR4 + CCR6 + Th17的浓度增加。同时,团队发现CD8 T细胞具有高浓度的细胞毒性颗粒,其中31.6%细胞为穿孔素阳性,64.2%细胞为颗粒溶素阳性,30.5%细胞为颗粒溶素和穿孔素双阳性。
2020年2月11日,清华大学免疫学研究所董晨团队在Immunity上发表题为Febrile temperature critically controls the differentiation and pathogenicity of T helper 17 cells 的文章,发现发烧能通过促进SMAD4的SUMOylation及入核,特异性地增强Th17细胞分化及IL-17的表达,提升其致炎能力,加重Th17细胞相关的小鼠模型自身免疫疾病症状。该发现首次揭示发烧和自身免疫疾病的相关性。

Doi:https://doi.org/10.1016/j.immuni.2020.01.006
在本文中,研究团队首先测试了不同T细胞亚群分化发育与温度的关系,发现在正常体温的基础上提升1-3°C,能显著增强Th17细胞的体外分化,但却不影响Th1,Th2及iTreg细胞的分化。研究者证实了发烧→热激反应通路→SMAD4 SUMOylation轴对温度敏感Th17细胞分化及其致病性的核心作用。
2005年,Harrington等根据分泌细胞因子的不同,首次提出了“TH17细胞”的概念。
TH17细胞在生物学功能上完全不同于以往的TH1、TH2细胞,不表达IL-4或IFN-γ,却特异性地高水平分泌IL-17,由此被命名为TH17细胞。
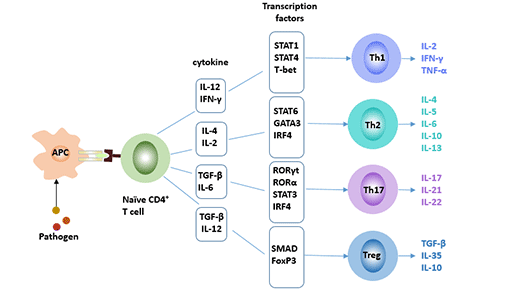
Figure 2 Four subsets of CD4+ T cells
人的Th17细胞可以使用CD4、CD161和CCR6的细胞表面标记来鉴定。Th17细胞的细胞标志物可分为两类:细胞内标志物和细胞外标志物。
细胞内标志物:IL-17A, IL-17F, IL-21, IL-22, RORα, RORγt, Stat-3。
细胞外标志物:CD3、CD4、CD38、CD161、CD194(CCR4)、CD196 (CCR6)、IL-1R、TGF-β。
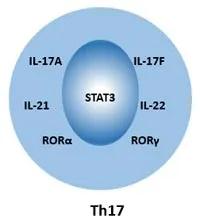
Figure 3 Cell Markers of Th17 Cells
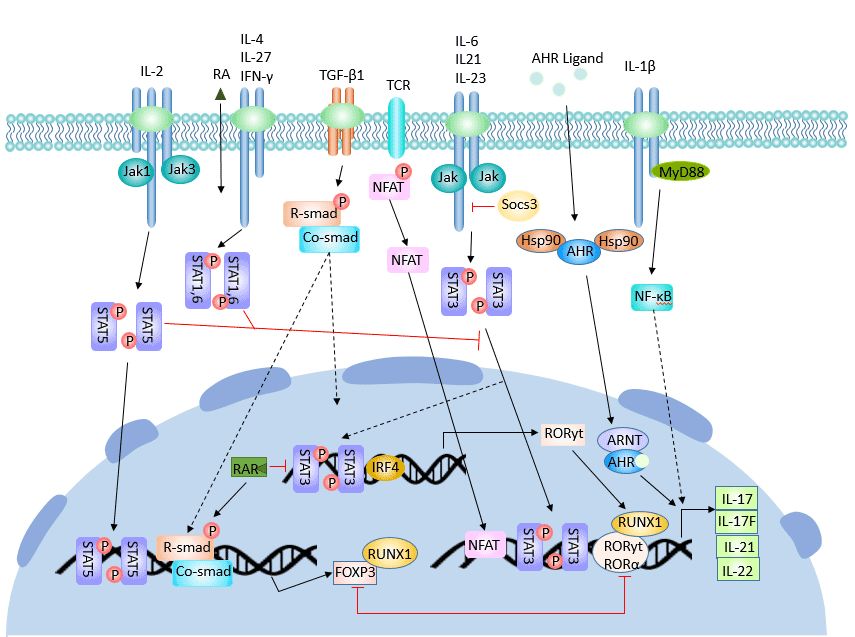
Th17细胞的分化受许多细胞因子和信号分子的调节。CD4+ T细胞在TGF-β和IL-6的协同作用下分化为Th17。CD4+ T细胞激活的第一步是T细胞受体的参与。TCR信号的强度决定Th1/Th2分化的方向。然而,TCR信号对Th17细胞分化的影响尚不清楚。 不同因素对Th17细胞分化的调节作用不同。转化生长因子β(TGF-β)、IL-6、IL-23、IL-21和RORγt在Th17细胞的分化和形成中起积极作用,而干扰素γ(IFN-γ)、IL-4和Socs3、Ets-1和IL-2抑制其分化。 Figure 4 The regulatory process of Th17 cell differentiation 延伸阅读: Differentiation of Th17 Cells
聚焦 Th17 细胞研究,或许能揭秘 COVID-19 病理进程,j9九游会登录入口首页CUSABIO提供 Th17 研究相关产品。疫情当前,初心未改,武汉j9九游会登录入口首页生物在疫情期间坚决做好稳生产、保供应,愿为您的新冠病毒研究保驾护航。
· ELISA KIT相关产品 ·
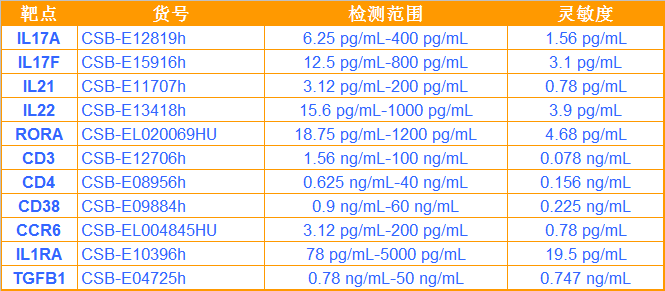
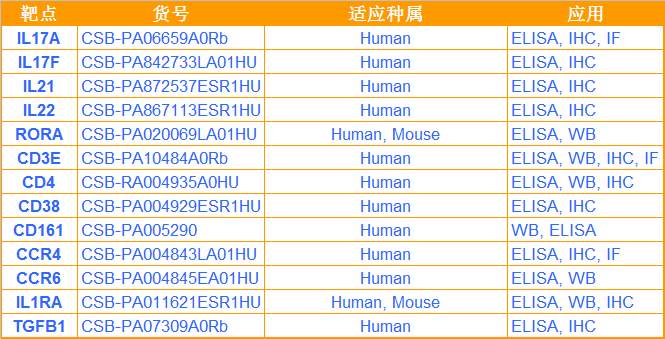
· 抗体相关产品 ·
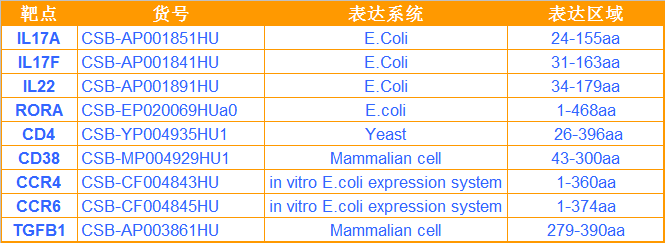
· 蛋白相关产品 ·
—END—
——j9九游会登录入口首页生物·让科研变得有温度!——
资源|基础研究数据库汇总 汇总|细胞器标志物通宵整理 精品推介|新兴治疗靶点BCMA 精品推介|EGFR最新研究进展及药物发展现状 精品推介|EphA3—细胞粘附和迁移的调节器 精品抗体|Oct4—胚胎干细胞多能性的看门人 精品抗体|GFAP—星形胶质细胞特异性标志物 精品抗体|肿瘤标志物CD146 精品抗体|CD31—多功能分子