抑瘤素M (OSM): 白介素IL-6细胞因子家族成员,肿瘤、骨代谢、慢性炎症性等疾病的潜力靶点?
日期:2023-09-03 08:41:33
细胞因子是由活化的免疫细胞产生的,包括促炎因子和抗炎因子,主要在免疫应答过程中起着重要的调节作用。许多与炎症相关的细胞因子被作为监测肿瘤或免疫性疾病风险的新靶点。白介素IL-6家族作为重要的促炎因子,在炎症反应中的作用日益凸显。近年来,随着IL-6家族被不断深入地研究,OSM作为IL-6细胞因子家族成员之一,OSM在肿瘤形成及免疫调节中的作用引起了越来越多的关注。大量的证据显示,OSM或许可以成为未来诊断、靶向治疗肿瘤等疾病的潜力靶点分子!
1. 白介素IL-6家族
白介素-6(interleukin-6,IL-6)家族是一组细胞因子(点击查看“细胞因子:白介素”专题),可以由多种细胞产生,它们以自分泌、旁分泌和内分泌的形式在信号转导中起作用。IL-6细胞因子家族包括IL-6、IL-11、IL-27、白血病抑制因子(LIF)、肿瘤抑制素M(OSM)、睫状神经营养因子(CNTF)、心肌营养因子1(CT-1)和心肌营养蛋白样细胞因子(CLCF 1)等。每个IL-6家族成员都在维持代谢、炎症和免疫稳态等生理调控中扮演着重要角色。众多研究发现,IL-6细胞因子家族成员在调控肿瘤的发生及发展过程中发挥着双向作用,即抗肿瘤和促肿瘤作用。近年来,IL-6细胞因子家族已成为肿瘤免疫学领域中的研究热点 [1-2]。
2. 什么是抑瘤素M(OSM)?
2.1 OSM的结构
抑瘤素M(Oncostatin-M,OSM)属于IL-6家族成员中的多效性细胞因子,在1986年首次从U937组织性淋巴瘤细胞中释放并分离出来,因其可抑制黑色素瘤细胞的增殖能力而得名。OSM基因位于22q12染色体上,由3个外显子和2个内含子组成,位置邻近于LIF。OSM蛋白全长含有239至263个氨基酸,折叠成一个与其他IL-6家族相似的四螺旋束长链蛋白(图1)[3]。人源OSM多肽含252个氨基酸残基,N-末端是由25个氨基酸残基构成的信号肽,C-末端由32个氨基酸残基构成。对于OSM的转录和表达,STAT5应答元件有重要作用,IL-2、IL-3、EPO、GM-CSF等多种细胞因子能激活STAT5,从而使OSM高表达;前列腺素E2/PG-E2能上调OSM转录 [3-5]。
2.2 OSM的表达与功能
OSM主要由激活的单核细胞、巨噬细胞、T淋巴细胞和树突状细胞分泌。OSM在维持造血微环境中起重要作用,它可通过调节G-CSF和SDF-1来维持祖细胞的造血功能。此外,OSM可调节中枢神经系统的发育、肝脏再生、诱导心肌细胞的去分化、调节内皮细胞产生其他细胞因子和生长因子,并刺激血管生成。目前的体外研究已证明,OSM具有多种生物学活性,在造血、细胞生长分化、炎症反应、代谢调控、肿瘤形成及免疫调节等方面发挥广泛的作用 [3-6]。
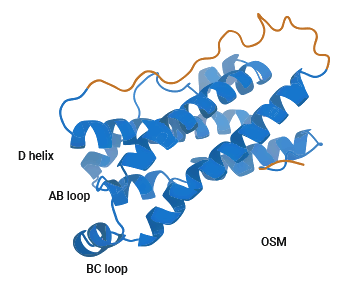
图1. OSM的结构 [3]
3. 什么是OSM的受体?
OSM与IL-6超家族内的其他几种细胞因子共有一个gp130受体亚单位,但其与gp130低亲和力结合。也就是说,这些IL-6细胞因子的受体基本上都包含信号传导受体亚基gp130糖蛋白。虽然gp130在所有细胞中都有表达,但单独存在的gp130无法与细胞因子结合。单个IL-6细胞因子家族成员的受体是细胞特异性的,这就意味着不同的细胞类型,可以表达特定的IL-6细胞因子家族成员受体 [7-8]。
与其它IL-6家族细胞因子不同的是,OSM可以通过两种不同的受体复合物发出信号,OSM受体分为I型和Ⅱ型两种。I型OSM受体(gp130/LIFRβ)是由一个gp130分子和一个LIF受体亚单位构成的异源二聚体,既可以与LIF结合,也可以与gp130结合而启动信号转导。Ⅱ型OSM受体(gp130/OSMRβ)是由一个gp130分子和一个OSM受体β亚单位构成的异源二聚体,Ⅱ型受体具有OSM特异性,不能结合LIF及家族中的其他细胞因子(图2) [8]。
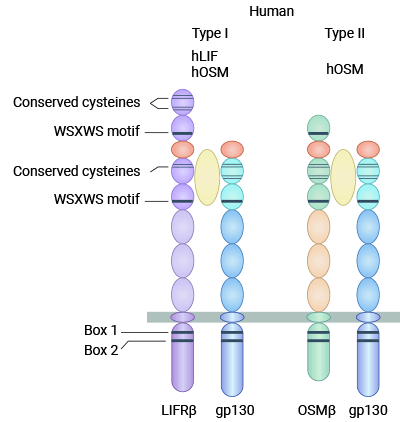
图2. I型OSM受体(gp130/LIFRβ)和Ⅱ型OSM受体(gp130/OSMRβ)[8]
4. OSM结合受体调节JAK/STAT3和MAPK信号通路
SM与不同的两种受体(gp130/LIFRβ;gp130/OSMRβ)结合后,会激活两个不同的信号通路:JAK/STAT3通路和丝裂原活化蛋白激酶(MAPK)通路。这两条通路在细胞内扮演关键角色,参与调节细胞的多种生物学响应(图3) [9]。
具体而言,JAK/STAT3通路通过与gp130/OSM受体β亚单位复合体结合来启动。这一过程导致受体复合体二聚体化和相互磷酸化,激活Janus激酶(JAK)。JAK激酶活化导致gp130胞浆区的酪氨酸残基磷酸化。然后,信号转导因子和转录激活分子(STAT)识别这些磷酸化的受体,促使STAT分子自身被磷酸化。这种磷酸化状态导致STAT形成同源和异源二聚体,并进入细胞核作为活性转录因子,对特定基因的表达产生影响 [9]。
另一方面,gp130酪氨酸残基磷酸化吸引酪氨酸磷酸酶,并为生长因子受体结合蛋白2(Grb2)提供一个连接点。这样一来,Grb2可以连接到SOS蛋白(son of sevenless),激活SOS。SOS可以促使原癌基因c-ras的产物Ras蛋白从GDP释放出来,与GTP结合,进而激活Ras。激活的Ras可以影响下游的Raf-1并激活它。Raf-1激活MAPK,并使其磷酸化并转变为活性状态。接着,激活的MAPK作用于细胞外信号调节蛋白激酶(ERK)1/2,使其活化。活化的ERK1/2进入细胞核,作用于特定的转录因子,影响基因的表达,因此发挥生物学活性 [9]。
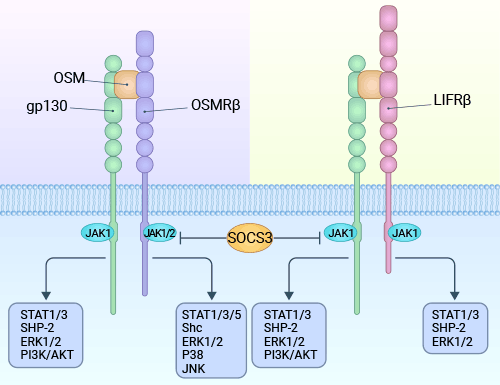
图3. OSM通过两种类型的受体传导信号:I型受体(gp130/LIFRb)和II型受体(gp130/OSMRb)复合物 [9]
5. OSM在疾病中的作用
OSM作为一种多功能的细胞因子,研究者对于OSM的功能及其作用机制还存在许多未知之处。OSM最初是在黑色素瘤中被发现可以抑制肿瘤细胞生长。随后的研究逐渐揭示,OSM在器官发育、组织损伤与再生等方面也起到重要的调控作用。然而,在不同的环境下,OSM对细胞增殖或分化可能起着不同甚至完全相反的作用。目前,对于OSM在疾病中的研究主要集中在肿瘤、骨代谢、造血以及慢性炎症性疾病方面。
5.1 OSM和肿瘤
OSM细胞因子在肿瘤中的作用并不是单一的。据报道,OSM所引起的这两种完全相反的效应与癌症的发展阶段或恶性程度之间存在一定的关联。总的来说,在正常上皮细胞和一些早期肿瘤中,OSM发挥着抑制增殖、抑制癌症进展的作用;然而,在恶性程度较高或具有转移倾向的肿瘤中,OSM的高表达则与不良预后相关。
以肝癌细胞为例,OSM通过激活STAT3信号途径、上调癌基因c-Myc表达的同时,也加速了细胞的衰老,从而最终表现为对肝癌细胞增殖的抑制作用(图4) [9]。然而,在晚期肿瘤中,OSM通常更多地表现为促进细胞增殖。具体地说,癌基因的激活所引发的细胞老化能够限制异常细胞的增殖,同时保持组织的健康状态,这是机体的一种防御机制。然而,癌基因诱发的细胞老化需要特定蛋白(如p53或Rb)的参与,而这些蛋白在晚期癌细胞中通常受到损害。因此,这可能解释了为何OSM在不同情况下会对肝癌增殖产生抑制或促进的不同效应 [9-10]。
此外,OSM还与其它多种肿瘤相关,包括黑色素瘤、肺癌细胞、乳腺癌、卵巢癌、胃癌等 [9-13]。例如,在乳腺癌中,OSM可以通过下调细胞膜E-cadherin表达、上调slug和snail表达而诱导癌细胞的间叶细胞表型 [14];在胶质瘤中,OSM所调控的间叶细胞表型可以增加胶质瘤细胞的迁移和侵袭能力,并且OSM表达水平同胶质瘤的恶性程度和患者的低生存率明显相关 [15];OSM在TGFβ信号通路的协同作用下促进胃肠胰神经内分泌肿瘤(GEP-NENs)细胞的迁移与侵袭 [16]。
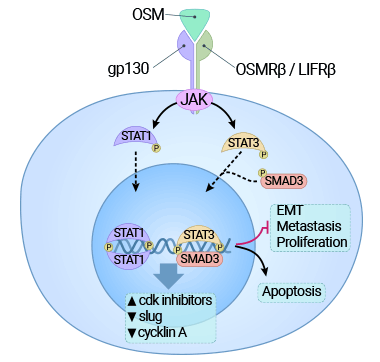
图4. OSM受体的结合激活JAK3/STAT1途径,并对癌细胞施加细胞毒作用 [9]
5.2 OSM和骨代谢相关疾病
已有研究证实,LIF和OSM均可调节大鼠颅骨细胞成骨细胞的分化过程。在体外实验中,小鼠成骨母细胞与骨形态发生蛋白BMP-2结合后,碱性磷酸酶增加,这提示在骨膜骨形成过程中,OSM能诱导募集BMP或其他因子。另有报道,当用小鼠OSM或人类OSM刺激时,小鼠颅骨外植体释放胶原蛋白,并调节骨保护素(Osteoprotegerin,OPG)的表达,从而抑制骨吸收活性。在类风湿关节炎患者的关节,由滑膜细胞产生的OSM能间接降解蛋白质,引发炎性介质PGE2产生,促进基质降解 [17-18]。
采用OSM/IL-1或OSM/TNF刺激模型,发现OSM在软骨细胞和滑膜成纤维细胞中诱导MMP-10,激活软骨细胞中的成纤维细胞活化蛋白-α,从而增强软骨代谢 [18]。此外,OSM抗体可以调节关节炎小鼠体内OSM与IL-1、TNF等细胞因子的相互作用,显著减少胶原蛋白的分解,减轻炎症反应,该发现为关节炎的治疗提供了新思路 [19]。
5.3 OSM和炎症性肠病
炎症性肠病IBD包括克罗恩病(Crohn’s disease,CD)和溃疡性结肠炎(Ulcerative colitis,UC)。OSM在炎性反应中发挥着促炎或抗炎作用。活动期CD患者结肠病变中OSM表达水平升高,但其也具有促进上皮修复的功能 [20]。另有报道,IBD患者受损的肠道粘膜高表达OSM及其受体OSMR。同时OSM还能诱导IL-6、ICAM-1等炎症因子的表达。对活动期UC患者分别予不同抗TNF药物治疗,结果发现抗TNF-α抗体Infliximab治疗无应答组粘膜OSM表达水平最高 [21-22]。因此,通过治疗性阻断OSM,可减少IBD发病时肠粘膜表达的OSM等相关炎症因子。这也表明OSM或可作为潜在的治疗靶点。
5.4 OSM和心血管疾病
陆续研究提示OSM可能参与心血管疾病的发生发展。OSM可刺激内皮细胞产生IL-6、G-CSF、GM-CSF及粘附分子,促进中性粒细胞黏附 [23-24]。OSM还通过调节COX-2、血管生成素-2/ANG-2促进微循环内皮细胞血管生成 [23-24]。此外,OSM影响血管平滑肌细胞,如刺激细胞增殖和分泌VEGF、IL-6和COX-2 [25]。在动脉粥样硬化中,OSM通过影响内皮细胞、血管平滑肌细胞和血管生成发挥复杂作用 [26-27]。在心肌梗塞和心室重构中,OSM的作用也复杂,可通过多种机制改善心脏功能,但在某些情况下可能产生不利影响 [26-27]。
5.5 OSM和其它疾病
除此以外,OSM还和多种代谢免疫以及神经性疾病相关 [28-29]。例如,OSM可单独或与其他GP130细胞因子共同作用,影响脂肪组织的正常代谢,造成脂代谢紊乱,进而诱导糖尿病 [30];OSM可通过Ras/细胞外信号调节激酶(Ras/ERK)和STAT5信号通路调节CCAAT增强子结合蛋白β(C/EBPβ)的表达来抑制脂肪细胞的分化,引起脂代谢紊乱 [31-32];OSMR缺陷的小鼠表达TRPV1/P2X3/OSMRβ的神经元也大量减少,OSMR缺陷的小鼠对机械刺激和热刺激等各种刺激的反应减退,提示OSM可作为神经保护性细胞因子,为探索OSM在CNS疾病中的治疗潜能提供了合理的基础 [33]。
6. OSM的临床研究前景
OSM是一种兼具多种生物活性的白介素IL-6家族细胞因子。众不同的是,OSM在体外和体内通过OSMRβ/gp130(II型OSM受体)途径得到特异性激活,从而施展其独特作用。尽管关于其多样生物学活性的作用机制以及与其他细胞因子之间的相互作用尚存待解之谜,但正是这些未知领域为研究者们提供了进一步深入探索的机遇。尽管如此,根据当前的研究成果,可以肯定的是,OSM激活剂以及其拮抗剂在临床疾病,如肿瘤、骨代谢、慢性炎症性等治疗领域有望呈现出广阔的应用前景。
为鼎力协助科研和药企人员针对OSM在多种免疫疾病和肿瘤中的临床应用研究,CUSABIO推出OSM活性蛋白(CSB-MP017260HU1),助力您在OSM机制方面的研究或其潜在临床价值的探索。
Oncostatin-M (OSM)蛋白
● Recombinant Human OSM, partial (Active) (Code: CSB-MP017260HU1)
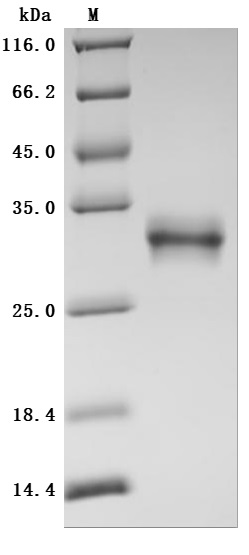
The high purity was greater than 95% as determined by SDS-PAGE.
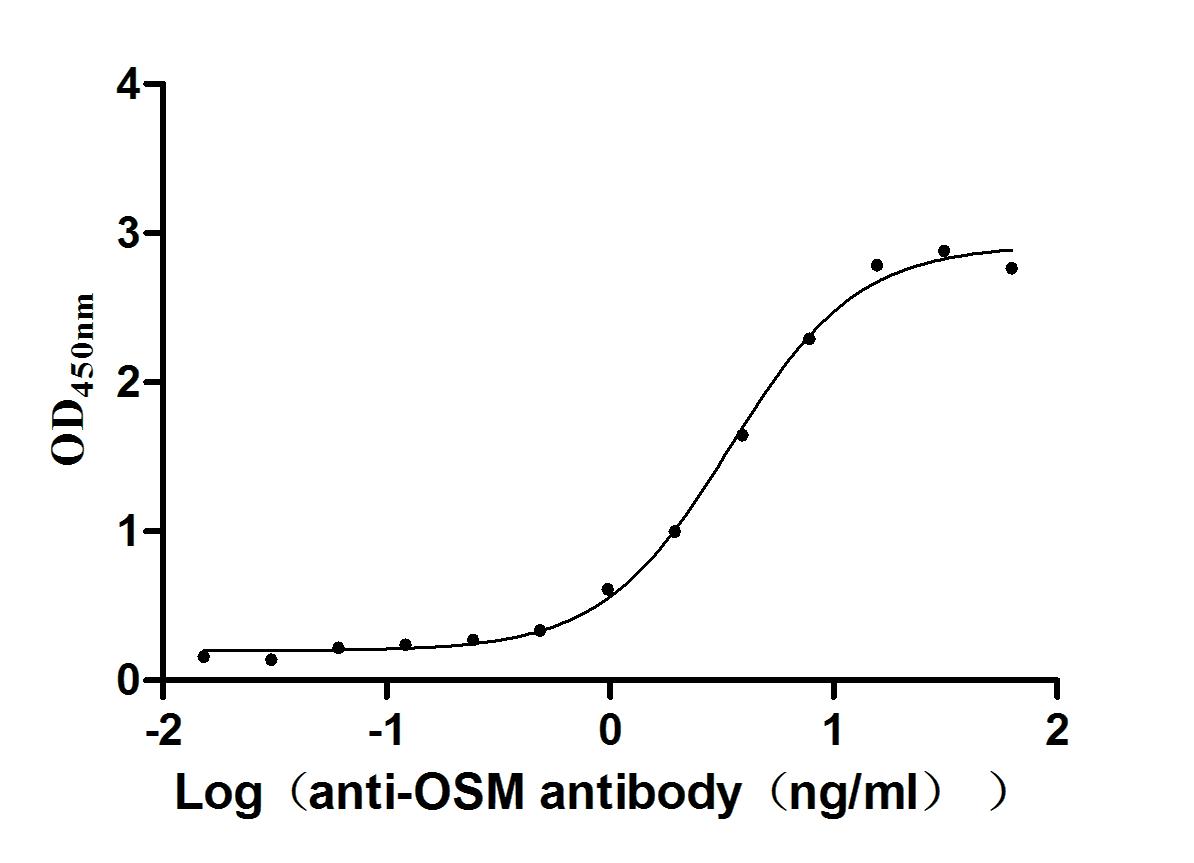
Immobilized Human OSM at 2μg/mL can bind Anti-OSM recombinant antibody (CSB-RA017260MA1HU). The EC50 is 3.048-3.860 ng/mL.
Oncostatin-M (OSM) 抗体
OSM Recombinant Monoclonal Antibody (Code: CSB-RA017260MA1HU)
参考文献:
[1] Tanaka, Toshio, Masashi Narazaki, and Tadamitsu Kishimoto. "Interleukin (IL-6) immunotherapy." cold spring harbor perspectives in biology 10.8 ( 2018): a028456.
[2] Jones, Simon A., Jürgen Scheller, and Stefan Rose-John. "Therapeutic strategies for the clinical blockade of IL-6/gp130 signaling." The Journal of clinical investigation 121.9 (2011): 3375-3383.
[3] Du, Qingqing, Yan Qian, and Weiwei Xue. "Molecular simulation of oncostatin M and receptor (OSM-OSMR) interaction as a potential therapeutic target for inflammatory bowel disease." Frontiers in Molecular Biosciences 7 (2020): 29.
[4] Bruce, A. Gregory, Peter S. Linsley, and Timothy M. Rose. "Oncostatin M." Progress in growth factor research 4.2 (1992): 157-170.
[5] Yoshimura, Akihiko, et al. "Mouse oncostatin M: an immediate early gene induced by multiple cytokines through the JAK-STAT5 pathway." The EMBO journal 15.5 (1996): 1055-1063.
[6] Botelho, Fernando M., et al. "Pulmonary expression of oncostatin M (OSM) promotes inducible BALT formation independently of IL-6, despite a role for IL- 6 in OSM-driven pulmonary inflammation." The Journal of Immunology 191.3 (2013): 1453-1464.
[7] Mosley, Bruce, et al. "Dual oncostatin M (OSM) receptors: cloning and characterization of an alternative signaling subunit conferring OSM-specific receptor activation." Journal of Biological Chemistry 271.51 (1996): 32635-32643.
[8] Grant, Susan L., and C. Glenn Begley. "The oncostatin M signalling pathway: reversing the neoplastic phenotype?" Molecular Medicine Today 5.9 (1999): 406-412.
[9] Masjedi, Ali, et al. "Oncostatin M: A mysterious cytokine in cancers." International Immunopharmacology 90 (2021): 107158.
[10] Caligiuri, Alessandra, et al. "Oncostatin M: From intracellular signaling to therapeutic targets in liver cancer." Cancers 14.17 (2022): 4211.
[11] M Stephens, Jacqueline, and Carrie M Elks. "Oncostatin M: potential implications for malignancy and metabolism. "Current pharmaceutical design 23.25 (2017): 3645-3657.
[12] Douglas, Andrea M., et al. "Oncostatin M induces the differentiation of breast cancer cells." International journal of cancer 75.1 (1998): 64-73.
[13] Junk, Damian J., et al. "Oncostatin M promotes cancer cell plasticity through cooperative STAT3-SMAD3 signaling." Oncogene 36.28 (2017): 4001-4013.
[14] West, N. R., J. I. Murray, and P. H. Watson. "Oncostatin-M promotes phenotypic changes associated with mesenchymal and stem cell-like differentiation in breast cancer." Oncogene 33.12 (2014): 1485-1494.
[15] Halfter, Hartmut, et al. "Inhibition of growth and induction of differentiation of glioma cell lines by oncostatin M (OSM)." Growth Factors 15.2 (1998): 135-147.
[16] Xue, Jingwen, et al. "TCF-3-mediated transcription of lncRNA HNF1A-AS1 targeting oncostatin M expression inhibits epithelial-mesenchymal transition via TGFβ signaling in gastroenteropancreatic neuroendocrine neoplasms." Aging (Albany NY) 13.10 (2021): 14065.
[17] Guihard, Pierre, et al. "Induction of osteogenesis in mesenchymal stem cells by activated monocytes/macrophages depends on oncostatin M signaling." Stem cells 30.4 (2012): 762-772.
[18] Hui, Wang, et al. "A model of inflammatory arthritis highlights a role for oncostatin M in pro-inflammatory cytokine-induced bone destruction via RANK/ RANKL." Arthritis Res Ther 7 (2004): 1-8.
[19] Le Goff, Benoit, et al. "Oncostatin M acting via OSMR, augments the actions of IL-1 and TNF in synovial fibroblasts." Cytokine 68.2 (2014): 101-109.
[20] West, Nathaniel R., et al. "Oncostatin M drives intestinal inflammation and predicts response to tumor necrosis factor-neutralizing therapy in patients with inflammatory bowel disease." Nature medicine 23.5 (2017): 579-589.
[21] Ito, Hiroaki. "IL-6 and Crohn's disease." Current Drug Targets-Inflammation & Allergy 2.2 (2003): 125-130.
[22] Verstockt, Sare, Bram Verstockt, and Séverine Vermeire. "Oncostatin M as a new diagnostic, prognostic and therapeutic target in inflammatory bowel disease (IBD)." Expert Opinion on Therapeutic Targets 23.11 (2019): 943-954.
[23] Albasanz-Puig, Adaia, et al. "Oncostatin M is expressed in atherosclerotic lesions: a role for Oncostatin M in the pathogenesis of atherosclerosis." Atherosclerosis 216.2 (2011): 292-298.
[24] Kubin, Thomas, et al. "The role of oncostatin M and its receptor complexes in cardiomyocyte protection, regeneration, and failure." International Journal of Molecular Sciences 23.3 (2022): 1811.
[25] Repovic, Pavle, et al. "Oncostatin-M induction of vascular endothelial growth factor expression in astroglioma cells." Oncogene 22.50 (2003): 8117- 8124.
[26] Gusakova, Anna M., et al. "Association of increased oncostatin M with adverse left ventricular remodeling in patients with myocardial infarction." Journal of Medical Biochemistry 41.4 (2022): 441.
[27] Han, Hui, et al. "Oncostatin M promotes infarct repair and improves cardiac function after myocardial infarction." American journal of translational research 13.10 (2021): 11329.
[28] Richards, Carl D. "The enigmatic cytokine oncostatin m and roles in disease." International Scholarly Research Notices 2013 (2013).
[29] Guo, Sen, et al. "Oncostatin M confers neuroprotection against ischemic stroke." Journal of Neuroscience 35.34 (2015): 12047-12062.
[30] Sanchez-Infantes, David, et al. "Oncostatin m is produced in adipose tissue and is regulated in conditions of obesity and type 2 diabetes. "The Journal of Clinical Endocrinology & Metabolism 99.2 (2014): E217-E225.
[31] Miyaoka, Yuichiro, et al. "Oncostatin M inhibits adipogenesis through the RAS/ERK and STAT5 signaling pathways." Journal of Biological Chemistry 281.49 (2006): 37913-37920.
[32] Zhou, Yue, et al. "Blockage of oncostatin M-induced LDL receptor gene transcription by a dominant-negative mutant of C/EBPβ." Biochemical Journal 397.1 (2006): 101-108.
[33] Morikawa, Yoshihiro. "Oncostatin M in the development of the nervous system." Anatomical science international 80 (2005): 53-59.












