CAR-T疗法是一种将患者自身的T细胞通过基因工程改造,使其表达特异性的嵌合抗原受体(CAR),从而增强其对癌细胞的识别和攻击能力的免疫疗法。该疗法在一些恶性肿瘤,特别是在某些难治性血液癌症的中展现出了惊人的疗效。
CAR生“万物”:从CAR-T到CAR-X
随着对免疫系统的深入了解,CAR技术的应用范围正不断拓宽,新型CAR细胞疗法的开发逐渐成为热点,如CAR-NK、CAR-M、CAR-Treg和CAR-γδ等。相比CAR-T疗法潜在的不良反应和无法应用于实体瘤治疗的痛点,这些新型CAR细胞疗法存在各自的优势,为免疫疗法的蓬勃发展注入了新的活力。
CAR的基本结构
无论是CAR-T,还是CAR-NK、CAR-M,它们都具有相似的CAR结构。CAR结构主要包括三个部分:胞外结构域、跨膜结构域和胞内结构域。
胞外结构域通常是一个单链可变片段(scFv),该片段由一个linker将抗体的可变重链(VH)和可变轻链( VL)连接形成,用于识别肿瘤抗原;一段铰链区将scFv与跨膜域相连,提供克服空间位阻的灵活性,以允许scFv进入靶向表位;跨膜结构域的主要功能是确保CAR稳定嵌入细胞膜;胞内结构域则包括共刺激结构域和信号转导结构域,用于激活和增强免疫细胞的反应。
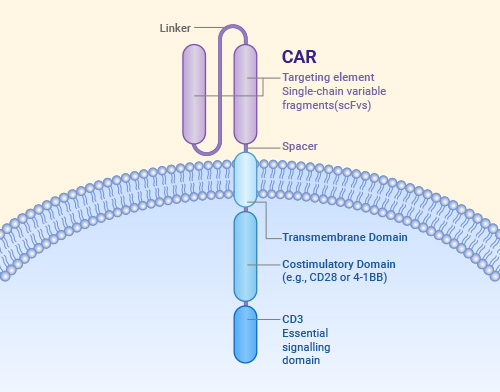
Structural elements of a chimeric antigen receptor(CAR)
Rodríguez-Lobato LG, et al. Front Oncol. 2020.
为什么进行CAR检测?
目前,随着越来越多的基于CAR技术的细胞疗法进入临床研究阶段,CAR表达部分的检测作为药物质控的关键环节,将直接影响治疗效果,相关法规更是对CAR阳性率的检测提出了明确要求。因此,为了确保从早研阶段的CAR细胞制备和功能测试、CMC阶段的细胞质量和纯度评估、临床测试阶段的细胞体内监测和PK研究等各个环节都能严格把控,开发准确、简便、通用的CAR阳性率检测试剂显得尤为重要。
现有的CAR的检测方法比较
常见的CAR检测方法包括针对人/小鼠IgG F(ab')2片段的多克隆抗体、抗独特型抗体、Protein L等,虽然各有优势,但也存在一些局限性,如需要针对每个CAR设计特异性抗体,成本较高,只能用于检测已知抗原等*。
| 检测方法 | 检测机制 | 优势 | 劣势 |
|---|---|---|---|
| Anti-human F(ab')2 pAb 和Anti-mouse F(ab')2 pAb | 结合IgG F(ab')2 片段 |
|
|
| Anti-idiotypic antibodies | 特异性结合scFv 抗原识别区 |
|
|
| rh-protein | 特异性结合scFv 抗原识别区 |
|
|
| Protein L | 结合抗体K轻链 |
|
|
| 本司产品 Linker-specific mAbs |
检测CAR连接子 |
|
|
*Linker-specific monoclonal antibodies present a simple and reliable detection method for scFv-based CAR NK cells. Mol Ther Methods Clin Dev. 2024.
j9九游会登录入口首页生物的linker-specific mAb产品
由于目前大多数CAR的构建体都含有Whitlow或G4S linker的单链可变片段(scFv),Whitlow (GSTSGSGKPGSGEGSTKG)linker主要用于针对血液恶性肿瘤的CAR构建,如CD19 CAR [1],而G4S(glycine4-serine)linker 则常用于针对实体瘤抗原的CAR,如HER2和CEA [2],若针对这两种linker开发特异性单克隆抗体则可以检测广泛的CAR。基于此技术背景,j9九游会登录入口首页生物现全新推出一组高效、通用性强的CAR阳性率检测工具--抗Whitlow Linker抗体和抗G4S Linker抗体。
● 产品列表
| 产品名称 | 产品货号 | 克隆号 |
|---|---|---|
| Whitlow linker Monoclonal Antibody | CSB-MA234468A0m | 18A3G5 |
| G4S linker Monoclonal Antibody | CSB-MA186062I1m | 11A12E7 |
| G4S linker Monoclonal Antibody | CSB-MA186062I2m | 12F11C10 |
| G4S linker Monoclonal Antibody | CSB-MA186062I3m | 14A10E7 |
● 产品优势
- 针对连接子特异性结合:特异性识别连接子序列,避免了与CAR其他区域的非特异性结合。
- 避免假阳性:由于linker-specific mAbs不与血清中的IgG或其他蛋白质结合,因此不会产生假阳性结果。
- 适用于大多数CAR: 大多数CAR都包含Whitlow或G4S 连接子,具有很强的通用性。
- 不受抗原特异性限制:不针对特定的抗原结合区域,可以检测不同抗原的CAR。
- 直接用于流式细胞术:无需复杂的实验步骤,操作简便,易于标准化。
- 兼容其他方法: 可以与其他检测方法(如rh-proteins)结合使用,提高检测的特异性和敏感性。
● 产品数据
(货号: CSB-MA234468A0m)
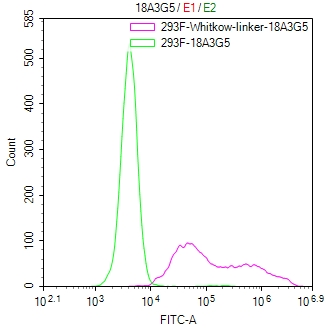
Untransfected HEK-293F cells (green line) and transfected scFv-based Anti-CD19 CAR containing a Whitlow/218 linker stable cells (red line) were stained with anti-Whitlow linker antibody (2µg/1*106), washed and then followed by FITC-conjugated anti-Mouse IgG Fc antibody and analyzed with flow cytometry.
(货号: CSB-MA234468A0m)
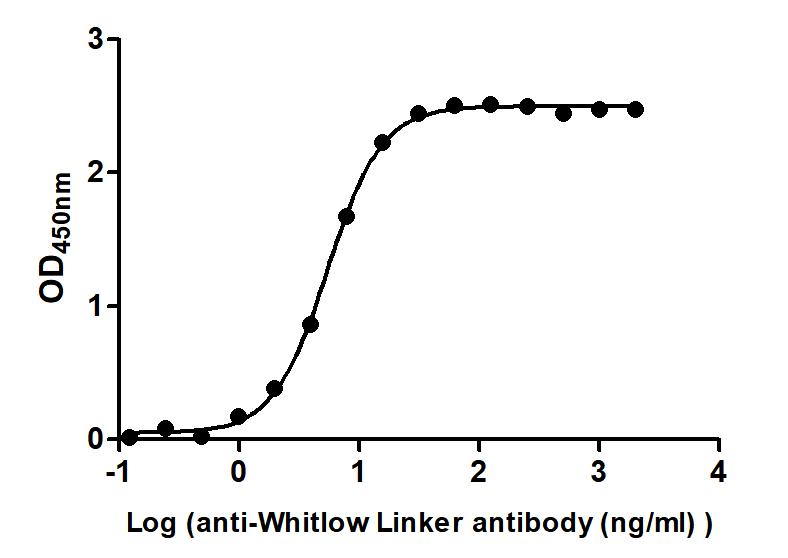
Immobilized scFv-based Anti-CD19 CAR recombinant antibody at 2 μg/mL can bind Anti-Whitlow linker antibody. The EC50 is 5.147 to 5.761 ng/mL.
(货号: CSB-MA186062I1m)
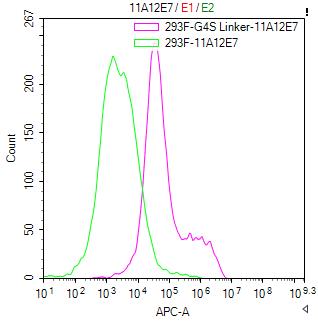
Untransfected HEK-293F cells (green line) and transfected scFv-based Anti-CD19 CAR containing a G4S linker stable cells (red line) were stained with anti-G4S linker antibody (2µg/1*106), washed and then followed by APC-conjugated anti-Mouse IgG Fc antibody and analyzed with flow cytometry.
(货号: CSB-MA186062I2m)
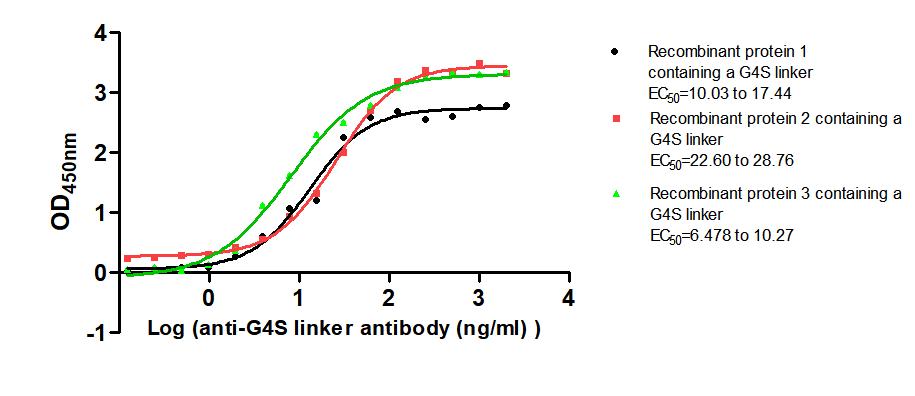
Immobilized Three recombinant proteins containing G4S linker at 2 μg/mL can bind Anti-G4S linker antibody. The EC50 is 10.03 to 17.44 ng/mL, 22.60 to 28.76 ng/mL and 6.478 to 10.27 ng/mL.
相关资源:
参考文献:
[1] B-cell depletion and remissions of malignancy along with cytokine-associated toxicity in a clinical trial of anti-CD19 chimeric-antigen-receptor-transduced T cells. Blood. 2012.
[2] CAR-T cell potency: from structural elements to vector backbone components. Biomark Res. 2022.