类器官的各大领域应用
与传统的2D细胞培养模型相比,3D培养的类器官包含多种细胞类型,可以形成功能性“微型器官”,更好地模拟器官组织的发生过程和生理病理状态。类类器官弥补了现有模型系统的某些局限性,提供了一个稳定的系统,易于培养和操作,同时在体内更能代表身体结构。
到目前为止,类器官培养物由于能够更好地模拟体内环境已用于多种组织,包括肠道、心脏、肝脏、胰腺、肾脏、前列腺、肺、视网膜和大脑。这无疑为肿瘤研究、疾病建模、药物筛选、再生医学、精准医学等领域介于动物和细胞水平之间提供了更好的解决方案。
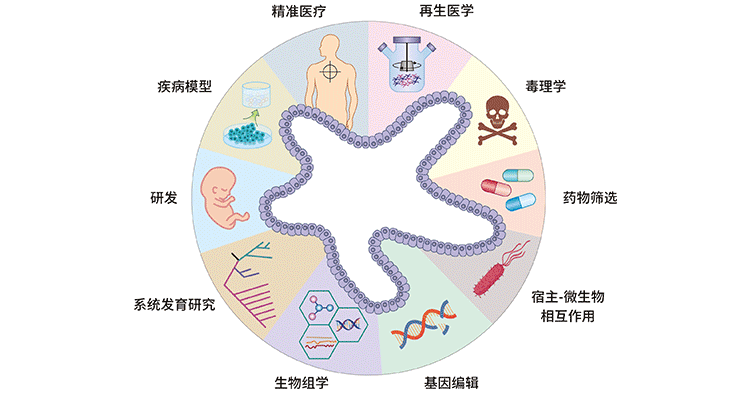
图1. 类器官技术的多样化应用
图片来源:https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7468890/
1、疾病模型
类器官为胚胎发育和成人组织的病理学建模提供了一个平台。类器官在功能和结构上与体内器官相似,也可用于模拟致病过程,包括传染性、遗传性和退行性疾病的模型。例如,如果胃类器官感染了幽门螺杆菌,则可以探索幽门螺杆菌的感染机制。包含病理的细胞可以使用基因编辑技术生成或从患者身上提取。已经使用 CRISPR/Cas9 敲除系统生成了肾脏类器官的病理模型。由人类诱导多能干细胞( iPSC) 产生的皮质类器官已被开发用于模拟 Miller-Dieker 综合征。
在疾病建模中,一些动物模型不能完全复现人类的体内状况,例如肺组织。由人体细胞生成的类器官除了伦理问题之外能克服动物模型原有的局限性。
类器官通常可以从正常人上皮细胞中获得,可用于体外模拟恶性肿瘤各个阶段的突变,揭示癌症基因组的复杂性以及在肿瘤发展中基因突变的重要作用,发现精准癌症治疗的药物靶点。此外,用于癌症研究的类器官,一个非常有用的发展是与免疫细胞共培养类器官。这些方法是接近生理性肿瘤微环境 (TME) 的重要步骤,并为基于免疫的治疗提供了平台。
肿瘤是一种复杂的疾病,无论是发病机制、转移机制,还是患者对治疗的反应和耐药机制,都有许多问题亟待探索。未来的研究需要不断完善对TME的模拟,建立更接近原始肿瘤性质的肿瘤类器官模型,从而对恶性肿瘤有更全面的认识。
2、药物发现与筛选
一般来说,新药的创制需要经过药物靶点选择、先导化合物鉴定、候选药物选择、动物安全性和有效性评价、人体临床试验等一系列过程。目前的药物研发主要以分子、细胞和动物为主。它涉及药物的毒性和有效性,因此必须经过动物到人类的实验过程,不能直接在人体上进行试验。然而,动物模型离人类还很远。因此,非常需要一种接近人体的疾病模型用于药物研发,以降低新药研发的成本和时间。类器官的应用可以大大提高这方面效率。
类器官的出现对药物发现具有很大的吸引力,因为它们可以用于捕捉疾病异质性的一系列亚型并且大规模生产进行长期存储,创建生物库。类器官生物库为测试药物安全性和有效性提供了机会。毒理学研究可用于评估安全性。对于功效测试,已经开发了几种高通量方法,可以在一周内获取药物反应结果。
类器官主要优势之一是在药物开发中可以生成正常的类器官并且利用它来筛选仅针对肿瘤细胞而不伤害健康细胞的药物。在临床试验中,不耐受的不良反应是导致药物失败的主要原因,包括肝毒性、心脏毒性和肾毒性。肝脏类器官可用于测试药物的肝毒性。药物相关的肝毒性主要由细胞色素 P450 酶介导,细胞色素 P450 酶的作用可以在接近生理水平的肝类器官中观察到。心脏毒性反应,如心律失常和心脏功能下降也可以在类器官中进行测试。此外,肾脏类器官也已用于药物毒理学研究。将类器官技术应用于临床前药物毒理学研究有助于降低药物临床试验的失败率,减少药物临床试验中不良事件的发生。类器官药物试验模型不能完全替代动物模型,但可以起到重要的补充作用。到目前为止,类器官已被用于治疗结肠癌和囊性纤维化等疾病的药物筛选。
3、再生医学与器官修复
除了体外应用外,类器官也被用于移植到其他生命体中研究以评估再生能力,成功的移植为类器官在再生医学中的应用铺平了道路。与植入式医疗设备相比,自体器官移植更不易受到磁场或物理攻击的影响,并且与同种异体器官移植相比,排斥的机会更低。类器官还可以通过用恢复的组织替换受损器官来在当代遗传基因异常的情况下进行基因校正。
4、个性化用药
预测患者对治疗的反应是类器官技术的另一个潜在应用。类器官提供了对个体患者疾病的独特见解,并显示出个性化治疗的潜力。通过在体外对患者来源的类器官进行一些治疗操作,可以根据类器官的反应来预测提供活检的患者对治疗可能出现的反应,从而为患者选择最合适的治疗方案。个性化医疗旨在通过在分子和药物基因组水平上更好地描述疾病,为每位患者制定有效的治疗方案。例如,测量来自囊性纤维化患者的直肠类器官中囊性纤维化跨膜电导调节剂的功能可以确定从囊性纤维化跨膜电导调节剂矫正治疗中的受益对象。对14例转移性结直肠癌患者1977个类器官癌相关基因的遗传分析显示,90%的体细胞突变与来自同一患者活检标本的类器官相同,与原始肿瘤对应的DNA拷贝数谱的相关系数为0.89。该实验表明,类器官可以很好地捕捉到原发肿瘤的遗传特性,这一实验为类器官在个体化医疗中的应用提供了有力的证据。
5、癌症免疫治疗
类器官与免疫细胞的体外共培养可以扩增免疫细胞,增强免疫应答,为后续的免疫治疗提供有力保障。此外,肿瘤微环境的研究也离不开类器官与免疫细胞等细胞的共培养技术。综上所述,来源于不同人体组织的类器官可用于药物研究、药物筛选和新药开发。它们还可以通过基因编辑来研究肿瘤出现和恶化的机制,并在体外用于预测患者对临床治疗的反应,从而帮助患者制定个性化的医疗计划。
虽然类器官有许多潜在用途,但目前仍存在很大的局限性。迄今为止建立的所有类器官系统在体内发育的可重复性方面仍需要改进。例如,视网膜类器官虽然很好地表现出典型的层状组织,但外部部分未能形成,光感受器官不能完全成熟以变得对光敏感。类似的,大脑类器官呈现了大脑发育中早期的特征,但随后的特征(如皮质层)还没有完全形成。并且需要开发更多的培养方法来提高生成效率,缩短类器官模型的培养周期,降低培养成本。
发育成熟问题似乎是类器官技术中的一个常见障碍,它是否会显着影响其治疗还有待观察。但确定的是,人类肠道类器官已被证明具有成熟肠道的特征并产生 Lgr5+ 成体干细胞。一旦异位移植成功用于治疗,其他类器官就可能会被诱导完全成熟,这些研究方向可能成为未来类器官研究的主要焦点。






